

JYMed Technology Co., Ltd. ten o pracer de anunciar que o seu produto, Tirzepatida, completou con éxito o rexistro do Arquivo Mestre de Medicamentos (DMF) coa FDA dos Estados Unidos (número DMF: 040115) e recibiu o recoñecemento da FDA o 2 de agosto de 2024.
Produción en masa con calidade estable
Segundo a alta dirección de JYMed Technology, a produción a granel do ingrediente farmacéutico activo (API) de tirzepatida pode alcanzar niveis de quilogramos. Os lotes de produción son estables e continuos, cunha variación mínima entre lotes, o que garante unha calidade consistente.
Efectos significativos na redución da glicosa e dos lípidos
A tirzepatida é o primeiro agonista do receptor GIP/GLP-1 de administración semanal aprobado no mundo. Como agonista de receptor dual, pode unirse e activar simultaneamente tanto o receptor do polipéptido insulinotrópico dependente da glicosa (GIP) como o receptor GLP-1 no corpo humano. Ademais de reducir os niveis de glicosa, reduce a inxesta de alimentos, o peso corporal e o contido de graxas, e regula a utilización de lípidos. Alén dos seus significativos efectos de redución da glicosa e de peso, as análises de subgrupos da serie de estudos SURPASS demostraron que a tirzepatida tamén mellora indicadores metabólicos como a presión arterial, os lípidos sanguíneos, o IMC e a circunferencia da cintura.
Aprobacións multinacionais e perspectivas prometedoras
Segundo a información relevante, o antiglicérido Mounjaro foi aprobado por primeira vez pola FDA dos Estados Unidos en maio de 2022 para o tratamento de adultos con diabetes tipo 2. Posteriormente, recibiu aprobacións na UE, no Xapón e noutras rexións. En novembro de 2023, a FDA tamén aprobou a indicación para a perda de peso coa marca Zepbound. En maio de 2024, entrou con éxito no mercado chinés. Dadas as súas amplas perspectivas de aplicación e os sólidos datos de investigación que o respaldan, a tirzepatida converteuse nun dos fármacos peptídicos máis destacados na actualidade. As súas vendas alcanzaron os 5.163 millóns de dólares en 2023 e só no primeiro trimestre de 2024 rexistrouse unhas vendas de 2.324 millóns de dólares, o que demostra unha taxa de crecemento asombrosa.
Acerca de JYMed

Shenzhen JYMed Technology Co., Ltd. (en diante denominada JYMed) fundouse en 2009 e especializouse na investigación, desenvolvemento, produción e venda de péptidos e produtos relacionados con péptidos. Cun centro de investigación e tres bases de produción principais, JYMed é un dos maiores produtores de API de péptidos sintetizados quimicamente en China. O equipo principal de I+D da empresa conta con máis de 20 anos de experiencia na industria dos péptidos e superou con éxito as inspeccións da FDA dúas veces. O sistema integral e eficiente de industrialización de péptidos de JYMed ofrece aos clientes unha gama completa de servizos, incluíndo o desenvolvemento e a produción de péptidos terapéuticos, péptidos veterinarios, péptidos antimicrobianos e péptidos cosméticos, así como apoio ao rexistro e á regulación.
Principais actividades empresariais
1. Rexistro nacional e internacional de API de péptidos
2. Péptidos veterinarios e cosméticos
3. Péptidos personalizados e servizos de CRO, CMO e OEM
4. Fármacos PDC (péptido-radionúclido, péptido-molécula pequena, péptido-proteína, péptido-ARN)
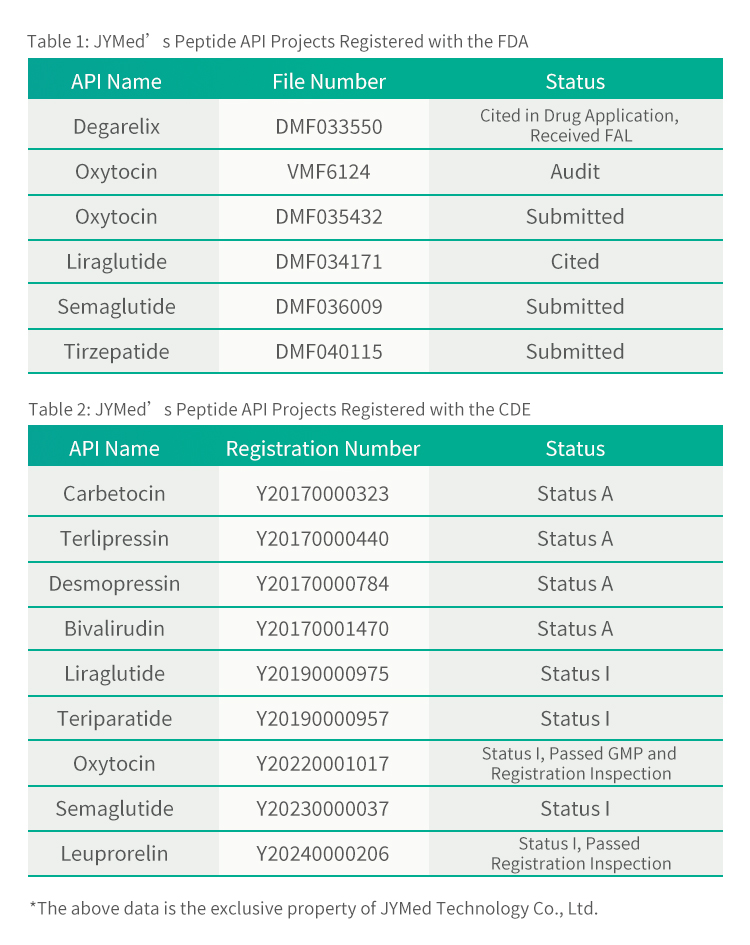
Ademais da tirzepatida, JYMed presentou solicitudes de rexistro á FDA e á CDE para outros produtos API, incluídos os populares fármacos da clase GLP-1RA, como a semaglutida e a liraglutida. Os futuros clientes que utilicen os produtos de JYMed poderán consultar directamente o número de rexistro da CDE ou o número de ficheiro DMF ao presentar as solicitudes de rexistro á FDA ou á CDE. Isto reducirá significativamente o tempo necesario para preparar os documentos da solicitude, así como o tempo de avaliación e o custo da revisión do produto.
Contacta connosco


Tecnoloxía Co., Ltd. de Shenzhen JYMed
Enderezo:Plantas 8 e 9, Edificio 1, Polígono Industrial de Innovación Biomédica de ShenzhenPark, no 14 Jinhui Road, subdistrito de Kengzi, distrito de Pingshan, Shenzhen
Teléfono:+86 755-26612112
Sitio web: http://www.jymedtech.com/
Data de publicación: 12 de agosto de 2024







